Физика
5.2.1. Планетарная модель атома
Ядерная модель атома (модель Резерфорда)
Большую роль в развитии представлений о строении атома сыграли опыты английского физика Э. Резерфорда.
Резерфорд и его сотрудники наблюдали прохождение α-частиц через тонкую золотую фольгу. Скорость α-частиц составила 107 м/с.
Экспериментальная установка позволяла наблюдать α-частицы, отклоненные золотой фольгой под разными углами.
В то время было известно, что α-частица имеет положительный заряд, равный +2е.
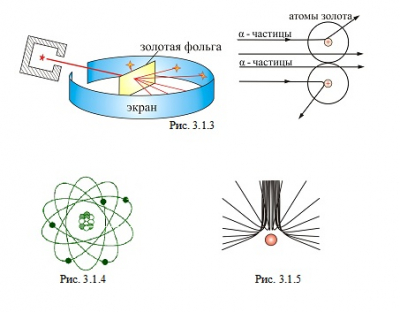
Опыт осуществлялся по схеме, изображенной на рис. 3.1.3.
Узкий пучок α-частиц испускался радиоактивным веществом и попадал на фольгу. Проходя через фольгу, α-частицы отклонялись на различные углы. Рассеянные частицы ударялись об экран, покрытый ZnS, и вызываемые им вспышки света, сцинцилляции, наблюдались в микроскопе. Микроскоп и связанный с ним экран можно было вращать вокруг оси, проходящей через центр фольги, т.е. можно было всегда измерить угол отклонения. Весь прибор помещался в вакуум, чтобы α-частицы не рассеивались при столкновении с молекулами воздуха.
В опыте обнаружилось, что некоторые α-частицы отклонялись на большие углы, до 180º. Резерфорд понял, что такое отклонение возможно лишь при встрече с положительно заряженной частицей большей массы. А малая вероятность отклонения на большие углы говорила, что эта положительная частица имеет малые размеры, порядка 10–14 м. Электроны, по мнению Резерфорда, движутся вокруг ядра.
Однако такая модель была в явном противоречии с классической электродинамикой, т.к. электрон, двигаясь по окружности, т.е. с нормальным ускорением, должен был излучать энергию, следовательно, замедлять скорость и падать на ядро. Таким образом, применение классической электродинамики к ядерной модели атома привело к полному противоречию с экспериментальными фактами. Согласно классической теории должны иметь место:
- непрерывная потеря электроном энергии в виде излучения электромагнитных волн и неустойчивость атома;
- существование только непрерывного спектра (спектральных линий не должно быть).
В действительности оказывается, что:
- атом является устойчивой системой;
- атом излучает энергию лишь при определенных условиях;
- излучение атома имеет линейчатый спектр, связанный со строением и свойствами его электронной оболочки.
Размеры ядер можно определить, используя дифракционное рассеяние при высоких энергиях, а также упругое рассеяние электронов или поглощение нейтронов.
Оказалось, что радиус ядра R » (10-14 – 10-15) м и зависит от числа протонов и нейтронов (нуклонов) в ядре (рис. 3.1.4).
Если электрон, ускоренный разностью потенциалов U, «нацелен» в край ядра, имеющего заряд Ze и радиус R, то, согласно классической механике, его угол отклонения определяется соотношением
\(tg\left( {\frac{\theta }{2}} \right) = {k_0}\frac{{Z{e^2}}}{{RpU}}\).
На рис. 3.1.5 изображена компьютерная модель процесса рассеяния электронов на ядре.