Физика
5.2.2. Постулаты Бора
Элементарная теория Бора
Бор высказал предположения, которые были названы постулатами Бора.
- Первый постулат (постулат стационарных состояний): электроны движутся только по определенным (стационарным) орбитам. При этом, даже двигаясь с ускорением, они не излучают энергию.
- Второй постулат (правило частот): излучение и поглощение энергии в виде кванта света (hn) происходят лишь при переходе электрона из одного стационарного состояния в другое. Величина светового кванта равна разности энергий тех стационарных состояний, между которыми совершается скачок электрона:
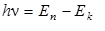
Отсюда следует, что изменение энергии атома, связанное с излучением при поглощении фотона, пропорционально частоте ν:
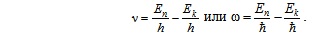
Правило квантования орбит: из всех орбит электрона возможны только те, для которых момент импульса равен целому кратному постоянной Планка:
 (3.1.3)
(3.1.3)
где n = 1, 2, 3,… – главное квантовое число.
Получим выражение для энергии электрона в атоме.
Рассмотрим электрон (рис. 3.1.6, а), движущийся со скоростью ʋ в поле атомного ядра с зарядом Ze (при Z = 1 – атом водорода).
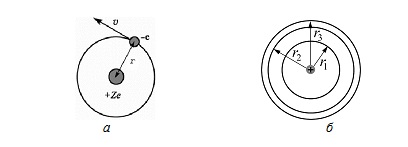
Рис. 3.1.6
Уравнение движения электрона имеет вид
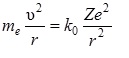 (3.1.4)
(3.1.4)
Из формулы (3.1.4) видно, что центробежная сила равна кулоновской силе, где 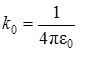 .
.
Подставим значение υ из (3.1.3) в (3.1.4) и получим выражение для радиусов стационарных орбит (рис. 3.1.6, б)
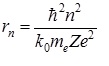
Радиус первой орбиты водородного атома называют боровским радиусом. При n = 1, Z = 1 для водорода имеем
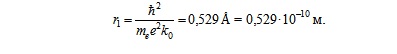
Внутренняя энергия атома слагается из кинетической энергии электрона (ядро неподвижно) и потенциальной энергии взаимодействия электрона с ядром:
\(E = \frac{{{m_e}{\upsilon ^2}}}{2} - \frac{{{k_0}Z{e^2}}}{r} = - \frac{1}{2} \cdot \frac{{Z{e^2}}}{{4\pi {\varepsilon _0}r}}\)
Подставим сюда выражение для радиуса стационарной орбиты и получим
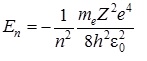 (3.1.5)
(3.1.5)
Здесь учтено, что постоянная Планка \(h = 2\pi \hbar \), т.е. \(4{\pi ^2}{\hbar ^2} = {h^2}\).
Для атома водорода, при Z = 1, имеем
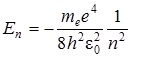 (3.1.6)
(3.1.6)
Из формулы (3.1.6) видно, что En принимает только дискретные значения энергии, т.к. n = 1, 2, 3, …
Схема энергетических уровней в (эВ), определяемых уравнением (3.1.6), показана на рис. 3.1.7.
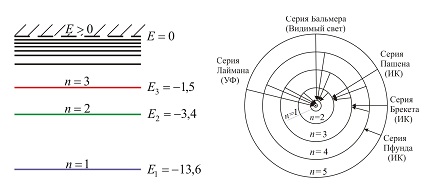
Рис. 3.1.7.
При переходе электрона в атоме водорода из состояния n в состояние k излучается фотон с энергией
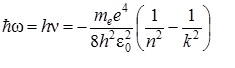
Частота излучения
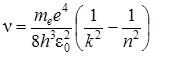
Получена обобщенная формула Бальмера, которая хорошо согласуется с экспериментом. Выражение перед скобками, носит название постоянной Ридберга:
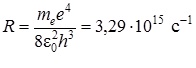
Серьезным успехом теории Бора явилось вычисление постоянной Ридберга для водородоподобных систем и объяснение структуры их линейчатых спектров. Бору удалось объяснить линии спектра ионизованного гелия. Он теоретически вычислил отношение массы протона к массе электрона (mp / me = 1847), что находится в соответствии с экспериментом и является важным подтверждением основных идей, содержащихся в его теории. Теория Бора сыграла огромную роль в создании атомной физики. В период ее развития (1913–1925) были сделаны важные открытия, навсегда вошедшие в сокровищницу мировой науки.
Однако, наряду с успехами, в теории Бора с самого начала обнаружились существенные недостатки. Главнейшим из них была внутренняя противоречивость теории: механическое соединение классической физики с квантовыми постулатами. Теория не могла объяснить вопрос об интенсивностях спектральных линий. Серьезной неудачей являлась абсолютная невозможность применить теорию для объяснения спектров атома гелия, содержащего два электрона на орбите, и тем более для многоэлектронных атомов (рис. 3.1.8).

Рис. 3.1.8.
Стало ясно, что теория Бора является лишь переходным этапом на пути создания более общей и правильной теории. Такой теорией и явилась квантовая механика.
Другие материалы по данной теме
Видео
Строение атома и теория Бора
Формула
hvnm = En - Em
Определение
Первый постулат Бора (постулат стационарных состояний)
