Химия
1.4.1. Классификация химических реакций в неорганической и органической химии
Классификация химических реакций в неорганической и органической химии - часть 2
3. По возможности протекать в обратном направлении на обратимые и необратимые.
Некоторые реакции, как например реакция горения этанола практически необратима, т.е. нельзя создать условия, чтобы она протекала в обратном направлении.
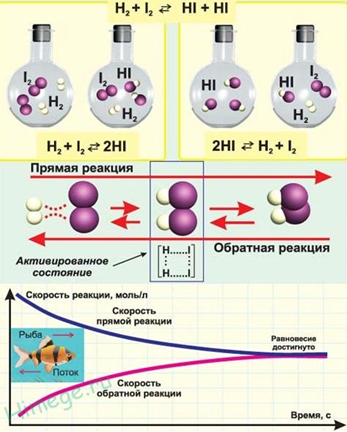
Однако, существует много реакций, которые в зависимости от условий протекания процесса могут протекать как в прямом, так и в обратном направлениях. Реакции способные протекать как в прямом, так и в обратном направлении называются обратимые.
4. По типу разрыва связи – гомолитические (равный разрыв, каждый атом получает по одному электрону)и гетеролитические (неравный разрыв – одному достается пара электронов).
5. По тепловому эффекту экзотермические (выделение тепла) и эндотермические (поглощение тепла).
Реакции соединения, как правило, будут экзотермическими реакциями, а реакции разложения – эндотермическими. Редкое исключение – реакция азота с кислородом эндотермическая N2 + O2 = 2NO – Q.
6. По агрегатному состоянию фаз.
- (реакция проходит в одной фазе, без границ раздела; реакции в газах или в растворах).
- (реакции, проходящие на границе раздела фаз).
7. По использованию катализатора.
Катализатор – вещество, ускоряющее химическую реакцию, но остающееся химически неизменным.
Каталитические без использования катализатора практически не идут и некаталитические.
Другие материалы по данной теме
Видео
4.3. Примеры решения задач
