Химия
3.6. Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров
Альдегиды и кетоны. Химические свойства. Реакции нуклеофильного присоединения
Химические свойства альдегидов и кетонов определяются наличием карбонильной группы.

Карбонильная группа содержит двойную углерод-кислородную связь. Поскольку подвижные p-электроны оттянуты к более электроотрицательному атому кислорода, он несёт частичный отрицательный заряд (δ-), а атом углерода – частичный положительный заряд (δ+). Таким образом двойная углерод-кислородная связь является полярной.
Положительно заряженный атом углерода карбонильной группы является местом нуклеофильной атаки, и большинство реакций присоединения являются нуклеофильными реакциями.
Реакции нуклеофильного присоединения
Следует напомнить, что нуклеофилы – это отрицательно заряженные ионы (CN–, OH–, CH3–) или молекулы, имеющие атом с неподеленной парой электронов, такие как вода, спирты, аммиак или амины.
Присоединение HCN
Присоединение синильной кислоты к альдегидам и большинству кетонов приводит к образованию циангидринов.

Присоединение самой синильной кислоты протекает очень медленно, поскольку HCN является слабым нуклеофилом. Добавление цианида калия или другого основания, которое может генерировать цианид-анион (более сильный нуклеофил) из HCN, значительно повышает скорость реакции присоединения. Присоединение происходит с учетом распределения электронной плотности:

Циангидрины содержат нитрильную группу, и их главное использование основано на том, что они подвергаются гидролизу, в результате чего образуются a-гидроксикислоты, в нашем примере получается молочная кислота или a-гидроксипропановая кислота.
Присоединение гидросульфита натрия
Гидросульфит натрия присоединяется к альдегидам и ко многим кетонам (особенно метилкетонам) с образованием продукта присоединения:
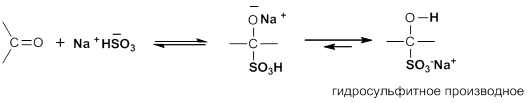
Кетоны, содержащие объемные заместители, в данную реакцию не вступают из-за пространственных затруднений.
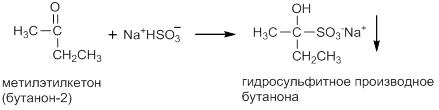
Практическое применение данной реакции в том, что она позволяет отделить карбонильные соединения от некарбонильных. Выпавшее в осадок гидросульфитное производное отфильтровывают и подкисляют, при этом происходит регенерация карбонильного соединения.

Другие материалы по данной теме
Видео
№ 94. Органическая химия. Тема 18. Карбоновые кислоты. Часть 6. Реакции химических свойств
