Химия
3.7. Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот
Амины. Реакции электрофильного замещения по кольцу
Группы NH2, NHR и NR2 выступают как мощные активаторы и орто-, пара-ориентанты в реакциях электрофильного замещения в ароматическом ядре. Распределение электронной платности в молекуле аналина хорошо иллюстрирует набор резонансных структур:
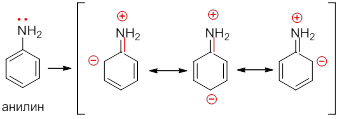
Ацилированная аминогруппа NHCOCH3 также обладает активирующим действием и ориентирует в орто- и пара-положения, но в меньшей степени, чем свободная аминогруппа, поскольку электронная пара атома азота находится в сопряжении не только с ароматическим кольцом, но и с карбонильной группой:
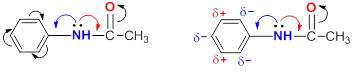
Протонированная аминогруппа NH3+ напротив, обладает сильным дезактивирующим эффектом и ориентирует электрофилы в мета-положения бензольного кольца.

Бромирование анилина
Активация бензольного кольца за счет наличия аминогруппы столь велика, что входящие атомы галогенов стремятся занять все свободные орто- и пара-положения. Анилин реагирует с раствором брома без нагревания и катализатора, образуя осадок 2,4,6-триброманилина:
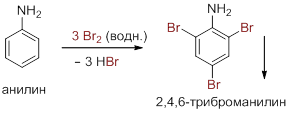
Сульфирование анилина
Анилин сульфируют концентрированной серной кислотой в две стадии. Вначале при комнатной температуре смешивают эквимолекулярные количества анилина и серной кислоты. Образовавшуюся соль нагревают в течение нескольких часов при 180-200 оС, при этом образуется 4-аминобензолсульфоновая (сульфаниловая кислота):

Сульфаниловая кислота –основа большого ряда сульфамидных препаратов, таких как белый стрептоцид, сульфадимезин, сульфодиметоксин, сульфаметоксазол и др.
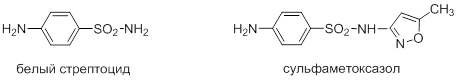
Другие материалы по данной теме
Видео
№ 170. Органическая химия. Тема 26. Аминокислоты. Часть 6. Схема химических свойств аминокислот
