Химия
3.4. Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола)
Механизм реакции галогенирования алканов
Механизмом реакции называют детальное описание химической реакции, которое включает элементарные стадии. Галогенирование алканов относится к реакциям цепногосвободнорадикального замещения (SR). Следует вспомнить, что свободный радикал – это атом или группа атомов, имеющих неспаренный (нечетный) электрон.
Общепринятый механизм галогенирования алканов может быть описан тремя основными стадиями:
Инициирование (зарождение цепи). Под действием УФ-облучения (ультрафиолетовое облучение) или при нагревании происходит гомолитический разрыв связи в молекуле хлора и она распадается на атомы:
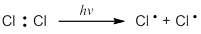
Развитие цепи (цепь последовательных взаимодействий свободных радикалов и неактивных молекул, в результате которых образуются новые молекулы и новые радикалы).
Образовавшиеся на первой стадии радикалы (атомы хлора) атакуют молекулы алканов, отрывая у них атом водорода:
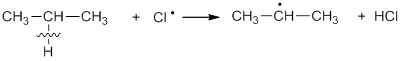
Образовавшиеся алкильные радикалы (в нашем случае это радикал изопропил) сталкиваются с молекулами галогена и гомолитически разрушают их. При этом получаются новые радикалы галогена и образуется алкилгалогенид:
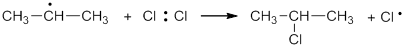
Обрыв цепи (соединении радикалов друг с другом с образованием неактивных молекул).
Столкновение двух короткоживущих частиц маловероятно, но все же оно иногда происходит и приводит к обрыву какой-либо стадии реакции:

В результате последней реакции образуется 2,3-диметилбутан. Это побочный продукт реакции.
Галогенирование алканов – пример цепной реакции. Цепная реакция включает ряд стадий, на каждой из которых образуется реакционноспособная частица, вызывающая следующую стадию.
Другие материалы по данной теме
Видео
Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола)
